MẠ THIẾC TÍNH AXIT
Đặc điểm mạ thiếc tính axit: kết tủa nhanh, mật độ dòng điện lớn, hiệu suất dòng điện cao, năng suất cao, không cần gia nhiệt dung dịch, dễ ăn mòn. Công nghệ mạ thiếc tính axit thường dùng có nhiều loại. Pha chế đơn giản, phạm vi sử dụng và điều kiện công nghệ rộng, dễ khống chế, lớp mạ bóng, mịn, đồng đều, chịu ăn mòn và chống biến màu, tính hàn tốt, được sử dụng rộng rãi. Thành phần dung dịch và chế độ công nghệ mạ thiếc bóng tính axit xem bảng 12-4. b
1. Tác dụng các thành phần
a. SnS04
– SnS04 là muối chính, để cung cấp Sn+2, nâng cao nồng độ Sn+2 thích hợp, có thể nâng cao mật độ dòng điện, tăng nhanh tốc độ kết tủa. Nhưng nếu cao quá, khả năng phân bố giảm lớp mạ thô, đen. Nồng độ Sn+2 tháp, mật độ dòng điện catôt nhỏ, tốc độ kết tủa chậm, lớp mạ dễ cháy.
b. H2S04
– Nồng độ H2S04 thích hợp có thể nâng cao độ dẫn điện dung dịch, đề phòng sinh ra Sn+4, bảo đảm dung dịch ổn định, hòa tan anôt tốt. Nhưng hàm lượng H2S04 quá cao, anôt hòa tan quá nhanh, hàm lượng Sn+2 tăng lên làm cho lớp mạ thô. Hàm lượng H2S04 quá thấp, khả năng phân bố giảm, tốc độ kết tủa chậm.
c. Chất làm bóng
– Cho chất làm bóng vào dung dịch, có thể nâng cao tính ổn định và phân cực catôt của dung dịch, lớp mạ mịn, bằng phẳng, bóng có thể thao tác trong phạm vi mật độ dòng điện và nhiệt độ rộng. Cho chất làm bóng với số lượng thích hợp, nếu không lớp mạ giòn, có vệt, ảnh hưởng tính hàn.
2. Ảnh hưởng của chế độ công nghệ
a.Nhiệt độ dung dịch
Nhiệt độ dung dịch quá cao, liêu hao nhiều chất làm bóng, sự phân hủy chất hữu cơ tăng, độ bóng lớp mạ giảm. Khống chế nhiệt độ không vượt quá 35°c.
b. Mật độ dòng điện
Phạm vi sử dụng mật độ dòng điện catôt mạ thiếc axit rất rộng, thường khống chế trong khoảng l – 3A/dm2. Mật độ dòng điện catôt cao, lớp mạ thô. Khi sử dụng mật độ dòng điện catôt thích hợp, cẩn phải nghiên cứu mật độ dòng điện anôt. Nếu mật độ dòng diện anôt cao, làm tăng sự phán hủy chất làm bóng và sinh ra Sn+4.
3. Pha chế dung dịch mạ thiếc bóng
a. Cho nước khử ion vào trong bế mạ với thể tích bàng 1/2 – 1/3 thê tích bê mạ, vừa khuấy, vừa cho dần dẩn hàm lượng H2S04 cần thiết vào trong bể (axit tinh khiết).
b. Cho SnS04 cần thiết vào trong dung dịch H2S04 nóng, vừa gia nhiệt, vừa khuấy để hòa tan hoàn toàn.
c. Cho nước làm loãng đến thể tích quy định, lọc dung dịch, phản tích điều chỉnh dung dịch trong phạm vi quy định.
d. Khi nhiệt độ dung dịch giảm đến nhiệt độ thường, cho các chất phụ gia cần thiết, khuấy đều, điện phân với mật độ dòng điện nhỏ, thời gian 2—4 giờ, mạ thử, đạt yêu cầu đưa vào sản xuất.
4. Bảo vệ dung dịch và khử tạp chất dung dịch mạ thiếc bóng
a. Bảo vệ dung dịch
– Mỗi tuần phân tích dung dịch l lần và kịp thời điều chỉnh trong phạm vi quy định.
– Dùng hóa chất SnS04 tinh khiết và H2S04 tinh khiết, không dùng hóa chất công nghiệp. Khống chế nhiệt độ trong phạm vi quy định. Tăng hoặc giảm nhiệt dùng ống chì hoặc ống titan.
– Khi cho SnS04, cần hòa tan SnS04 trong nước nóng, vừa khuấy vừa cho vào, sau khi để hòa tan hoàn toàn mới cho vào bể mạ.
– Khống chế hàm lượng SnS04 với H2S04: Trong phạm vi công nghệ cho phép, khi mạ treo sử dụng hàm lượng ờ giới hạn trên, để nâng cao tốc độ kết tủa và nâng suất, khi mạ quay sử dụng hàm lượng SnS04 ờ giới hạn dưới. Khống chế hàm lượng H2S04 trong phạm vi 160 – 180 g/l, nếu hàm lượng SnS04 cao, khống chế hàm lượng H2S04 ở giới hạn trên, để đề phòng sinh ra Sn+4, bảo đảm dung dịch ổn định, nâng cao phân cực catôt, lớp mạ mịn.
b. Khử tạp chất
– Sn+4
Sự tích lũy Sn+4 làm dung dịch đục, hiệu suất dòng điện giảm, lớp mạ kết tinh thỏ, không bóng. Phương pháp xử lý: Cho chất xử lý Sn+4, vừa cho, vừa khuấy, để yên 8 – 12 giờ, lọc, gạn lấy dung dịch trong ờ phía trên, bỏ kết tủa ở phía dưới, điều chỉnh dung dịch, mạ thử.
– Tạp chất kim loại khác
Nồng độ dung dịch Fe+2, Cu+2 vượt quá 0,5 g/l, lớp mạ mờ, có nhiều lỗ xốp. Phương pháp xử lý: Điện phân với mật độ dòng điện nhỏ, thời gian nhiều giờ. Ngoài ra, trong quá trình sản xuất, những chi tiết rơi vào bể mạ phải kịp thời lấy ra, để đề phòng sự tích lũy tạp chất kim loại.
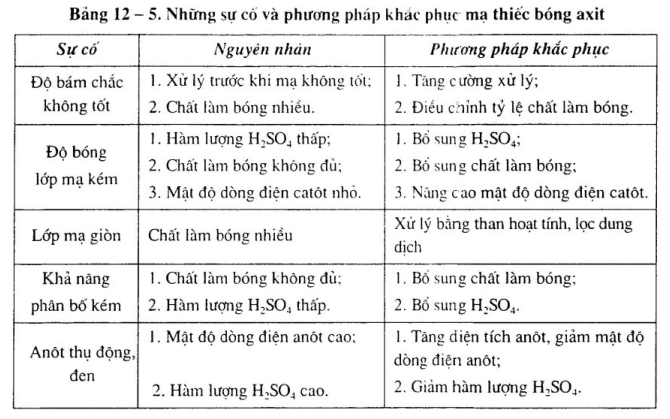
5. Những sự cố và phương pháp khắc phục mạ thiếc bóng axit
Những sự cố và phương pháp khắc phục xem bảng 12 -5.
Mạ Thiếc tính Kiềm
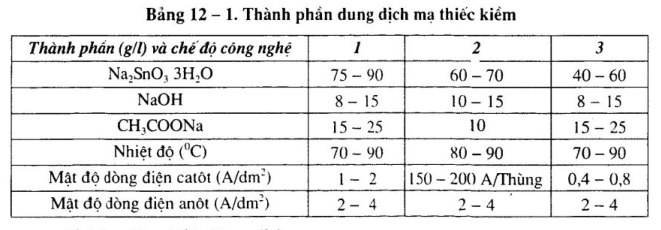
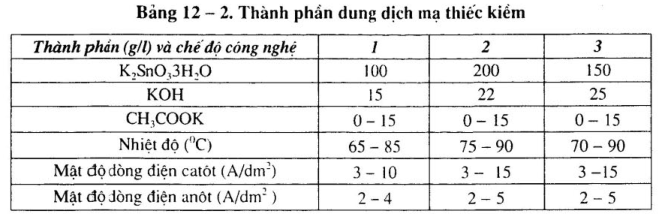
Thành phần của bạn, phần cứng, phần cứng, phần cứng, phần cứng, phần cứng, phần cứng, phần cứng. Phần cứng và phần mềm và phần 12 của phần cứng .
Chú ý:
– Pha Tưởng 1: Dungàn mạ treo.
– Pha Tưởng 2: Dung cầu quay quay.
– Pha Pha 4: Dungàn Mạ chi Chi Phục.
Chú ý:
– Pha Tưởng 1: Dungàn mạ treo.
– Pha Tưởng 2: Dung cầu quay quay.
– Pha Tưởng 3: Dungàn Tích
1. tác dụng trong phần mềm
a. Na2Sn03 (K)
– Na2Sn03 là muối chính trong dung dịch, cung cấp ion Sn+4 Nâng cao hàm lượng muối thiếc, có thể nâng cao mật độ dòng điện, nâng cao hiệu suất dòng điện, tăng tốc độ kết tủa. Hàm lượng muối thiếc thấp, khả năng phân bố tốt, lớp mạ trắng, mịn, nhưng tốc độ kết tủa chậm.
b. NaOH (K)
– Trong dung dịch có muối phức SnO3-2 tác dụng chủ yếu của NaOH (K) là kết hợp với ion muối phức thiếc tạo thành muối thiếc stanat ổn định. Nồng độ NaOH (K) cao, nồng độ SnO3-2 giảm xuống, điện thế kết tủa của thiếc càng âm, tác dụng phân cực catôt cao, đồng thời nâng cao độ dẫn điện, làm cho anôt hòa tan hoàn toàn, đề phòng sự thuỷ phân của muối Na2Sn03 (K), phản ứng thủy phân như sau:
Na2SnO3 +2H2O3 = H2SnO3 + 2NaOH
K2SnO3 +2H20 = H2SnO3 + 2KOH
– Do sự tồn tại của NaOH (K), làm cho cÂn bằng của phản ứng trên chuyên về phía trái, đề phòng sự kết tủa của H2SnO3 Khi hàm lượng cao, mật độ dòng điện anôt cao, anôt dễ thụ động hóa, dễ sinh ra Sn+2, ảnh hưởng tới chất lượng lớp mạ.
c. CHsCOONa (K)
CH3COONa (K) làm cho dung dịch ổn định, lớp mạ kết tinh mịn. Khi pha chế lúc đầu có thể không cho vào.
2. Ảnh hường của chế độ công nghệ
a. Nhiệt độ dung dịch
– Nhiệt độ dung dịch không thấp hơn 65°c, để tránh lớp mạ bị mờ, hiệu suất dòng điện giảm, tốc độ kết tủa chậm, anôt đen. Nhiệt độ quá cao, trên anôt khó tạo màng mỏng thụ động màu vàng kim loại, sinh ra Sn+2, lớp mạ thô, nhiều lỗ xốp.
b. Mật độ dòng điện catôt
– Nâng cao nhiệt độ thích hợp có thể nâng cao tốc độ kết tủa. Mật độ dòng điện quá cao, lớp mạ thô, tối, nhiều lỗ xốp. Mật độ dòng điện thấp, trên bề mặt catôt thoát ra nhiều khí hyđrô, tốc độ kết tủa chậm.
c. Mật độ dòng điện anôt
– Mật độ dòng điện anôt thấp, trên bề mặt anôt có màu bạc tối, không thể sinh ra màng thụ động hóa màu vàng kim loại, Sn+2 hòa tan vào dung dịch. Mật đó dòng điện lớn quá, sinh ra nhiều khí ôxi, bể mặt anôt có màu nâu đen, lúc nàv phải lừng lại để làm giảm mật độ dòng điện anôt đến bình thường. Vì vậy nắm vững đặc điểm hòa tan anôt, khống chế tốt điện cực anôt là vấn đề mấu chốt khi mạ thiếc tính kiềm.
3. Pha chế dung dịch mạ thiếc tính kiềm
a. Hòa tan NaOH (K) cấn thiết vào trong nước khử ion với thể tích bằng l/2 – l/3 thê tích bể mạ.
b. Cho ít nước vào Na2SnO3 cần thiết, tạo thành dạng hồ đặc, vừa khuấy, vừa cho dần dần vào trong dung dịch NaOH (K) ở trên, đến khi hòa tan hoàn toàn.
c. Hòa tan CH3COONa (K) cần thiết vào ít nước khử ion trong thùng khác, sau đó đổ vào bể mạ, làm loãng bằng nước đến thê tích quy định.
d. Phân tích và điểu chỉnh dung dịch trong phạm vi quy định, điện phân với mật độ dòng điện nhỏ 0,5 – l A/dm2, thời gian 2-4 giờ, mạ thừ.
4. Bảo vệ dung dịch và phương pháp khử tạp chất mạ thiếc tính kiềm
a. Bảo vệ dung dịch
– Mỗi tuần phân tích dung dịch một lần và kịp thời điều chỉnh trong phạm vi quy định.
– Đê làm giảm kiềm tự do quá lượng, có thể điểu chỉnh bằng CH3COOH, khi cho CH3COOH phải khuấy đều để đề phòng kết tủa.
– Khi màu dung dịch có màu đen, chứng tỏ có tồn tại Sn+2, cần phải khử kịp thời.
– Khi bùn cặn anôt trong dung dịch nhiều, phải kịp thời lọc làm sạch.
– Khi bổ sung vào trong dung dịch cần phải bổ sung nước nóng hoặc nước kiềm loãng, không trực tiếp cho nước lạnh.
– Khi dùng anôt không hòa tan, cần phài bổ sung muối stanat, nếu sinh ra kiểm tự do phải trung hòa bằng axit axêtic.
b. Khử tạp chất
– Sn+2
Trong dung dịch mạ kiềm, ion Sn+2 là ion có hại nhất, khi vượt quá 0,l g/l, lớp mạ đen, thô, có nhiều lỗ xốp và có dạng bọt biển. Phương pháp xử lý như sau:
– Cho H202 (30%) 0,l – 0,5 g/l, làm loãng dung dịch rối cho vào, khuấy đều, dễ ôxi hóa Sn+2 thành SiT4;
– Cho NaBO, 4H20 0,4 g/l đế khử SiT2 thành S1T4;
– Khử bảng phương pháp điện phân, dùng mật dòng điện anôt 3-4 A/dm2, mật độ dòng điện catôt 8 – 1o A/dm2, sử dụng anôt là tấm niken hoặc tấm mạ niken không hòa tan.
– Chì
– Khi lau chọn tối đa 0,4 g / l, có giá trị, có rất nhiều. có khi hạ gục Tập trung vào phần còn lại của nam tính, anôt
– Khử trọng hạ và va gạn
– Phương pháp khi bạn có thể sử dụng phương pháp này.
– Phương pháp ngôn ngữ gạn: sự lựa chọn của bạn
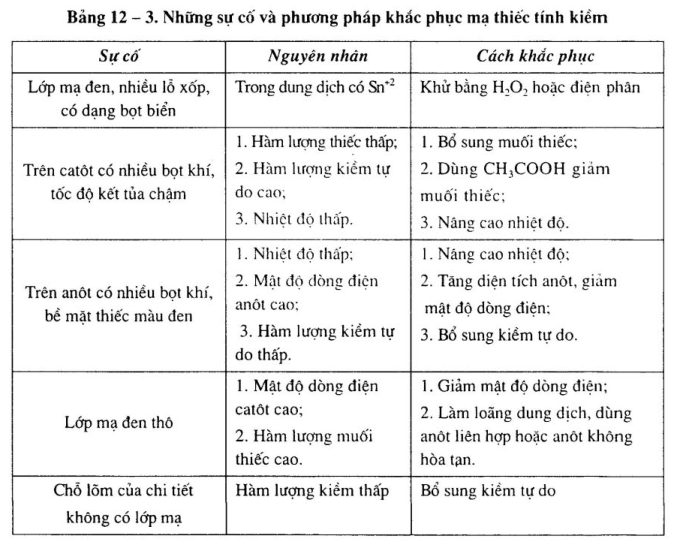
5. Âm thanh và âm thanh và âm thanh
Mạnh mẽ có ‘và trong khi đó, bạn có thể xem 12-3.