XỬ LÝ NƯỚC THẢI KIM LOẠI NẶNG
Ngoài nước thải crôm, nước thải còn chứa nhiều ion kim loại nặng như: niken, đồng, kẽm, cacđimi… Để xử lý kim loại nặng thường dùng các phương pháp: phương pháp kết tủa, điện phân, trao đổi ion, kỹ thuật phân ly màng, cô đặc, bay hơi…
1. Phương pháp kết tủa hóa học
a. Phương pháp kết tủa hợp chất hyđrôxit
– Cho vào nước thải chất kết tủa tính kiềm (NaOH, Na2CO3, vôi…), làm cho ion kim loại phản ứng với gốc OP-1 tạo thành hợp chất hyđrôxit không tan, do đó bị phân ly ra. Phương pháp kết tủa là phương pháp điều chỉnh, khống chế pH.
– Nước thải có ion kim loại nặng, về cơ bản có thể điều chỉnh pH để kết tủa phân ly. Khi ion kim loại nặng ở dạng phức chất, trước tiên phải phân hủy phức chất, sau đó điều chỉnh pH để kết tủa.
– Công nghệ trung hòa kết tủa có hai loại: trung hòa kết tủa một lần và trung hòa kết tủa phân đoạn. Mấu chốt của phương pháp trung hòa kết tủa là khống chế tốt pH, cần căn cứ tính chất của nước và loại kim loại nặng phải loại bỏ mà chọn công nghệ trung hòa kết tủa.
b. Phương pháp kết tủa hợp chất sunfua
– Cho vào nước thải hợp chất sunfua như Na2S , (NH4)2S… làm cho ion kim loại và ion lưu huỳnh phản ứng, sinh thành hợp chất sunfua kim loại khó hòa tan, được loại bỏ đi. Thứ tự kết tủa hợp chất sunfua như sau: Hg+2, Ag+1, As+3, Bi+3 , Cu+2, Pb-2, Cd+2,Sn+2, Zn+2, Co+2, Ni+2, Fe+2, Mn+2. hợp chất sunfua có vị trí ở phía trước, độ hòa tan rất nhỏ, xử lý dễ dàng.
2. Xử lý nước thải niken
– Phương pháp xử lý nước thải niken gồm có các phương pháp: phương pháp kết tủa, phương pháp trao đổi ion, phương pháp thẩm thấu ngược. Ở đây giới thiệu đơn giản phương pháp trao đổi ion. Trong nước thải có niken, niken tồn tại ở dạng ion Ni+2, pH nước thải vào khoảng 6. Dùng phương pháp này, do thế trao đổi của Ni+2 so với Cu+2, Fe+2 thấp, yêu cầu hàm lượng Ni+2 trong nước thải không thấp hơn 200 – 400 mg/l, do đó cần bể thu hồi nước thải niken mới đạt yêu cầu. Nhựa trao đổi thường dùng là DK – 110, DK – 116, nhựa 732 axit mạnh sau khi chuyển về dạng Na thì sử dụng. Trong thực tế sản xuất, thường xứ lý nước thải niken 2 cột cố định.
Phương pháp thao tác:
– Nước thải sau khi lọc, cho vào cột A, tiên hành trao đổi ion. Khi cột A có ion niken lọt ra (dùng Dimethyl gliôxim để kiểm tra), lắp cột B song song với cột A, sau khi cột A hấp phụ đã bão hòa, ngắt nguồn nước, tiến hành tái sinh.
– Cột B tiến hành trao đổi, khi có ion niken lọt ra, cột A mắc song song vừa được tái sinh, cột B đã hấp phụ bão hòa, tái sinh cột B, cho cột A tiến hành trao đổi. Thao tác tái sinh: Trước tiên rửa ngược bằng nước, để loại bỏ chất huyền phù trong nhựa, dùng N1SO4 12% làm chất tái sinh, lượng dùng gấp 1,3 – 1,4 lần thể tích nhựa. Nước rửa ngược và nước rửa thường ra ngoài, dùng Dimethyl gliôxim để kiểm tra không hiện ra màu đỏ là được.
3. Xử lý nước thải có đồng
Phương pháp xử lý nước thải có đồng, dùng phương pháp kết tủa hóa học, phương pháp cô đặc bay hơi, phương pháp trao đổi ion. phương pháp hấp thụ than, phương pháp phân ly màng và phương pháp điện phân. Sau đây giới thiệu phương pháp trao đổi ion, phương pháp kết tủa – điện phân màng.
a. Phương pháp trao đổi ion
– Nước thải mạ đồng piro phôtphat có thể loại bỏ báng nhựa trao đổi ion âm tính kiểm, như nhựa số 731 loại muối sunluaric. dùng hỗn hợp chất tái sinh là (NH4)2S04 15% và KOH 3%, có thể tái sinh hiệu quả. Dùng nhựa trao đổi ion dương tính axit mạnh (số 732) để trao đổi hấp phụ Cu+2 trong nước, sau khi nhựa hấp phụ đã bão hòa. dùng axit lái sinh, sau đó trở thành dạng Na2S04.
– Nước thải mạ đồng xianua, dùng cột trao đổi ion âm đê loại bỏ xianua, thông thường dùng nhựa trao đổi ion âm kiểm mạnh polistron sổ 711 để trao đổi, tái sinh bằng axit mạnh, khi phản ứng tái sinh, sinh ra khí HCN rất độc. dùng thiết bị hấp phụ kín khít đế hấp phụ (dung dịch NaOH), như vậv có thể giải quyết được sự ô nhiễm cùa HCN, mà còn thu hồi được NaCN. Sau đó loại bỏ đóng trong hợp chất xianua, bằng cột trao đổi ion dương. Chất thu hồi được cho vào bể mạ. Phương pháp xử lý như trên, hàm lượng đồng trong nước thải dưới 1 mg/l.
b. Phương pháp kết tủa– điện phân màng
Nguyên lý cơ bản:
Cho ion đồng hoặc các ion kim loại khác kết tủa, thông qua điện phân, làm kết tủa biến thành kim loại.
– Kết tủa hóa học: lon đồng trong nước thái ở điều kiện trung tính hoặc kiềm yếu sinh thành kết tủa hợp chất hyđrôxit.
– Điện phân màng: Cho kết tủa Cu(OH): vào trong buồng anôt của bể điện phân màng, buồng catôt cho dung dịch ion đồng, buồng anôl, catôt dùng màng tách ra, anôt là chì, catôt là kim loại dễ tách lớp mạ ra. Chỉ cần bảo đảm nồng độ ion đồng, pH và nhiệt độ dung dịch, ờ mật độ dòng điện thích hợp, kim loại được tách ra.
– Thành phần dung dịch và điều kiện công nghệ như sau: buồng catôt hàm lượng dung dịch là: CuS045H20 200 – 250 g/l, pH < 1 ,2 nhiệt độ 30 – 40°c, nguyên liệu catôt là đồng tinh khiết, buồng anôt gồm kết tủa đồng, cho lượng nước gấp 10 lần, anôt là chì, mật độ dòng điện 1 – 3 A/dnr, màng là tấm nỉ, dùng phương pháp này có thể xử lý nước thải có niken và kẽm.
4. Kỹ thuật xử lý nước thải hỗn hợp
a. Công nghệ mới xừ lý nước thải mạ: phương pháp điện phân sắt
– Nước thải được bơm cho vào cột xử lý sắt hoạt tính, sinh ra một loạt phản ứng, loại bỏ các loại ion kim loại trong nước thải. Nước thải qua kết tủa hoặc dùng thiết bị phân ly nước cặn bã, nước chảy ra ngoài hoặc dược dùng lại.
b. Chất thu hồi kim loại nặng cao phân tử (DTCR)
– DTCR là dạng nhựa chất lỏng, sau khi phản ứng với ion kim loại nặng trong nuớc thải, tạo thành muối không hòa tan trong nước, cho thêm chất hữu cơ hoặc vỏ cơ, sẽ sinh thành kết tủa không hòa tan, đạt mục đích loại bỏ ion kim loại nặng trong nước thải. DTCR có thể tạo thành phản ứng với ion kim loại năng như: Hg+2, Cd+2, Pb+2 Mn+2 Cu+2, Ni+2, Zn+2, Cr+3 Cr+6… tạo thành muối không hòa tan trong nước, tiến hành xử lý một lần được tất cả các ion kim loại nặng.
5. Xử lý ion kim loại có kẽm
a. Phương pháp hóa học
– Dùng axit để điều chỉnh nước thải có kẽm tính kiềm, có pH = 8,5 – 9, sinh thành Zn(OH)2 kết tủa, cho kiềm để hòa tan kết tủa, được dùng lại cho bể mạ. Dùng kiềm để điều chỉnh nước thải tính axit có pH = 8,5 – 9, sinh thành Zn(OH)2 kết tủa, chất kết tủa cho axit để tạo thành ZnS04 hoặc ZnCl2, được dùng lại cho bể mạ. – Để nâng cao độ tinh khiết của hóa chất thu hồi, nước rửa phải dùng nước cất hoặc nước trao đổi ion. Thời gian phản ứng kết tủa vào khoảng 20 phút, nồng độ nước thải có kẽm không bị hạn chế, nước thải sau khi xử lý có thể sử dụng lại được hoặc thải ra ngoài đạt tiêu chuẩn.
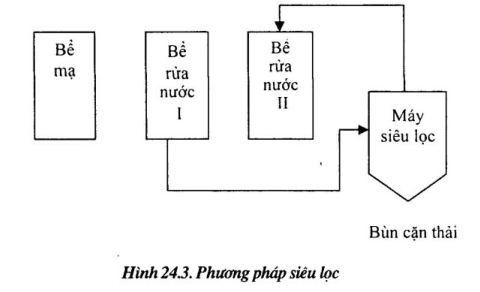
b. Phương pháp siêu lọc Khi pH = 8 – 10, ion kẽm sinh thành Zn(OH) kết tủa tương đối ổn định, trong máy siêu lọc, Zn(OH)2 bị màng lọc chặn lại, đạt mục đích lọc loại bỏ, dung dịch lọc được sử dụng lại tuần hoàn ở bể rửa, nước thải ra, hàm lượng kẽm dưới 0,5 mg/1.
Quy trình công nghệ xem hình 24.3.
6. So sánh các phương pháp xử lý
Xem bảng 24 – 1.